其他師資
專任師資
兼任師資
合聘師資
退休師資
教師簡介


癌症代謝是指癌細胞在能量與營養物質的使用方式上與正常細胞不同的現象,這種代謝重新編程(metabolic reprogramming)是在癌症發展過程中的重要特徵之一。這些代謝特性不僅促進腫瘤生長,還會改變腫瘤微環境,有助於癌細胞的免疫逃逸與轉移。其中,癌症代謝與抗藥性之間具有密切的關聯。癌細胞為了適應藥物治療所產生的壓力,常透過改變其代謝途徑來提高存活能力與抵抗治療效果。舉例來說,某些癌細胞在接受標靶治療或化療後,會增強醣解作用(如Warburg effect)或改變能量產生途徑,轉向依賴胺基酸代謝或脂肪酸氧化,藉此繞過藥物影響的關鍵路徑。此外,代謝的改變也能調節細胞內抗氧化能力,使癌細胞更能抵抗藥物引發的氧化壓力與細胞凋亡。這些現象顯示癌症代謝不僅是腫瘤生長的驅動力,也是癌症抗藥性的重要機制之一。近年來,隨著對腫瘤代謝特性的理解加深,以其作為靶點的治療策略日益受到重視,成為新型抗癌方法的發展重點。因此,本實驗室致力於探討癌細胞在治療抗性中所涉及的代謝途徑,並以此為基礎發展相關治療策略,期望成為克服抗藥性的潛在途徑。
1.發掘代謝物(胺基酸、脂肪、碳水化合物)在癌症發展過程中所扮演的角色
代謝物 (metabolites) 長期以來被視為能量代謝反應中的中間產物,以滿足細胞釋放或儲存能量的需求。然而,最近的研究發現,除了能量的需求,代謝物亦可以作為生長因子、免疫調節因子、表觀遺傳調控因子等,來調控各種細胞功能。在癌症發展過程中,代謝扮演了至關重要的角色。以最著名的瓦氏效應(Warburg effect)為例,此一現象揭示了癌細胞採用一種不同於正常細胞的代謝方式來適應其生存需求。此外,癌細胞的這種代謝變化還可能影響腫瘤微環境,進一步促進癌症的轉移。 因此,本實驗室其中一個研究方向是揭示代謝物在腫瘤進程中所扮演的具體角色。有系統性地從不同層面 (基因轉錄、轉譯及蛋白質功能) 來研究代謝物如何影響腫瘤的形成和發展。我們期望能夠藉由揭示這些代謝產物在癌症進程中的具體功能,來探討它們如何調控腫瘤細胞的增殖、轉移以及對治療的反應。因為這不僅有助於闡明癌症的機制,還可能為開發新的癌症治療策略提供關鍵的線索。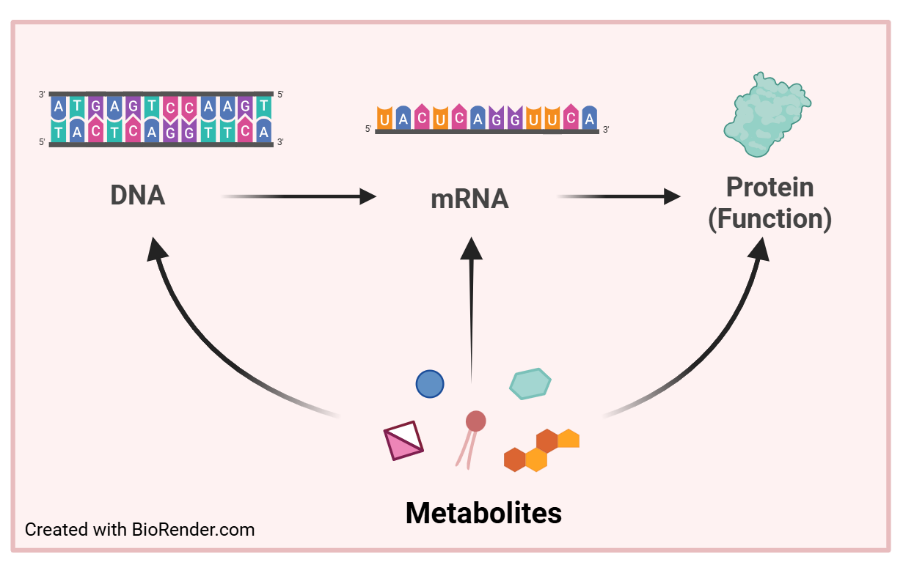
2.鐵凋亡機制調控
鐵凋亡(ferroptosis)是一種由於細胞內鐵依賴性的脂質過氧化作用而引發的細胞死亡形式。這一過程與傳統的細胞凋亡不同,具有獨特的生物化學特徵。近年來,鐵凋亡在癌症進程中的作用受到越來越多的關注。研究發現,一些癌細胞通過增強抗氧化劑的表達來抵抗鐵凋亡,提高對化療藥物的耐受性。於是,通過誘導鐵凋亡克服癌症抗藥性如今已成為研究熱點,一些藥物和小分子被開發來抑制GPX4或干擾鐵代謝,觸發鐵凋亡並消除對傳統治療不敏感的細胞。將誘導鐵凋亡的化合物與常規化療聯合使用,可增強治療效果,尤其是對多重藥物抗性的癌症。然而,關於癌細胞如何調控鐵凋亡的具體機制,至今仍未完全明瞭。本實驗室的研究主題之一就是通過在不同層面上(包括基因轉錄、轉譯及蛋白質功能)有系統地研究鐵凋亡的調控機制。我們希望能夠通過誘導鐵凋亡,為克服癌症治療中的抗藥性開拓一條具前景的治療途徑,包括開發創新的聯合療法以及尋找生物標誌,以識別最適合接受此類療法的患者。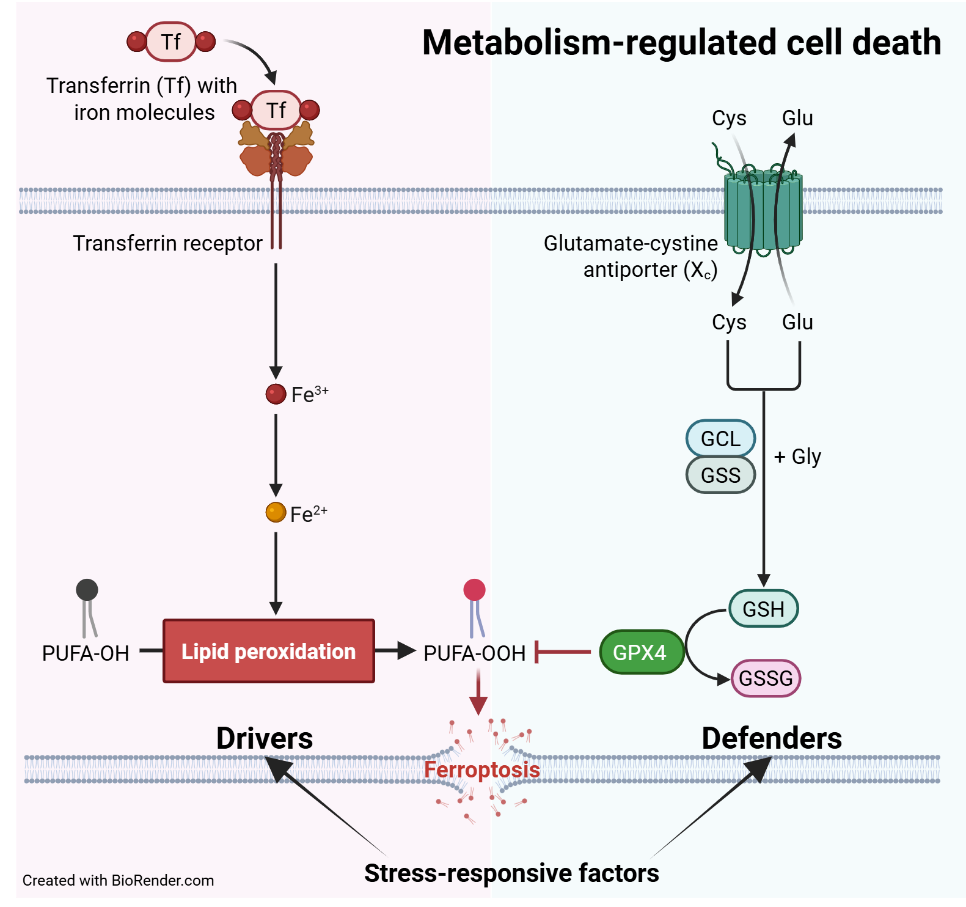

南加州大學
遺傳分子細胞學
博士
國立中央大學
生命科學系
碩士
東海大學
畜產系
學士
代表著作
期刊發表
其他師資
專任師資
兼任師資
合聘師資
退休師資